Стали известны результаты испытаний COVID-вакцины от Johnson & Johnson
16.01.21 - 16:07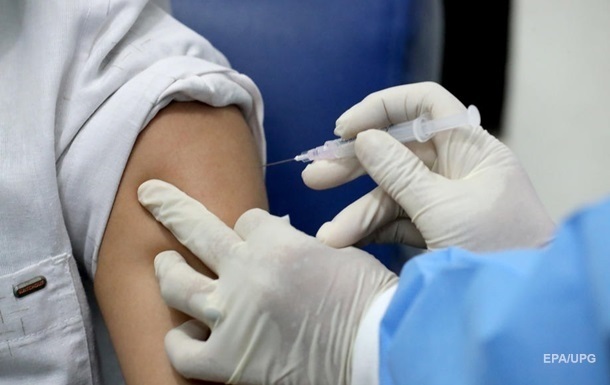 Вакцина от Johnson & Johnson на финишной прямой испытаний
Вакцина от Johnson & Johnson на финишной прямой испытаний
Препарат в ходе клинических испытаний показал до 100% эффективности при побочных эффектах сопоставимых с другими вакцинами.
Антикоронавирусная вакцина-кандидат Ad26.COV2.S от компании Johnson & Johnson (разработка ее "дочки" – Janssen) успешно прошла фазу I / IIа клинических испытаний. Результаты исследований опубликованы в журнале New England Journal of Medicine.
Отмечается, что основа препарата – нереплицирующийся вектор из аденовируса человека 26-го типа (Ad26), геном которого модернизирован так, чтобы производить S-белок SARS-CoV-2. Другими словами, создатели взяли безобидный для человека вирус одной из "простуд", лишили его возможности размножаться в клетках, и вооружили белками-шипами коронавируса – чтобы "раздражать" иммунитет и обучать его бороться с настоящим коронавирусом.
В исследовании случайным образом были распределены 805 здоровых взрослых участников 18-55 лет (когорта №1) и >65 лет (когорта №3). Они получали дозу 5х1010 вирусных частиц (низкая доза) или 1х1011 (высокая) на 1 мл, или плацебо. Применена как однократная, так и двухдозовая иммунизация: поверялась безопасность и реактогенность (побочные эффекты) каждого режима.
В когорте №2 собираются более долгосрочные данные для сравнения одно- и двухдозовой схем; результаты испытаний в ней будут опубликованы позже.
Выяснилось, что самые частые "нежелательные явления" были типичными: боль в месте инъекции, утомляемость, головная боль, миалгия, а также лихорадка. "Побочки" были менее распространены в когорте пожилых, у вакцинированных низкой дозой, и после второй дозы. В целом, реактогенность Ad26.COV2.S была сопоставима с другими аналогичными вакцинами, причем при второй дозе – меньше, чем у Pfizer/BioNTech и Moderna.
К исходу первого месяца после первой дозы нейтрализующие антитела были у более 90% привитых, у 100% к концу второго месяца, и продолжали расти. Этот эффект наблюдался независимо от дозы или возраста. Вторая доза повышала количество антител до трех раз.
Что касается Т-клеточного ответа, то спустя две недели лимфоциты типа CD4+ нашли у 76-83% людей из когорты №1 и у 60-67% среди пожилых. Отмечен четкий крен в Т-клетки типа Th1, что является положительным моментом, так как уход в Th2-ответ ведет к возможному усилению симптомов.
Клинические испытания отчетной фазы стартовали 22 июля, а фаза III (заключительная) началась 7 сентября на 60 000 добровольцев с однократным введением и 15 ноября на 30 000 по двухдозной схеме с интервалом в 57 суток.
